
新冠肺炎的大流行让全世界的人们意识到追踪接触者的重要性。为了能够控制病毒感染的大爆发,需要知道谁被感染,以及这个人什么时候在哪里被感染。对这种知识的缺乏迫使世界上大多数国家实施了限制和封锁措施,这导致了严重的社会混乱和全球经济衰退。
快速检测测试设备的成功研发使人们能够在关键的、并且无法封闭的社会领域进行接触追踪,例如医疗保健和食品供应行业。价格低廉的测试方法也使人们能够快速进行自我诊断,并在得知感染的情况下进行自我隔离。这也有助于减缓病毒的传播。韩国和德国已经成功地利用这种测试在更大范围内减缓了新冠肺炎在群体中的大流行 (参考文献1).
快速检测新冠肺炎的一种可能的测试手段是基于侧向层析测定法(LFA),也称为侧向流免疫层析测定法(LFIA)或免疫层析试验。我们在超市就可以买到的标准验孕棒可能就是LFA最常见的一种应用。LFA 为许多疾病和病症提供了一种便宜的、相对可靠的、稳定的和易于使用的测试手段(参考文献2).
本文是系列博客(由两部分组成)的第一篇文章,下面我们将使用 COMSOL Multiphysics 软件来了解 LFA 设备的功能以及工程师在设计这些设备时可能遇到的挑战。
LFA 快速检测测试背后的原理
如果对这些快速检测测试背后的机制进行仔细研究,我们可以看到,这些测试设备是相当先进的,并且是一个非常强大的微型实验室。
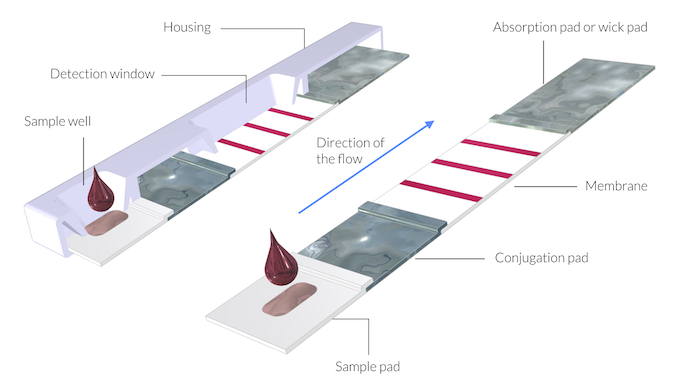
快速检测测试装置示意图。这里为了显示测试装置的结构,膜和平板的厚度被放大了 5 倍。平板和膜的组装件称为测试条。
测试条由以下几部分组成(如上图所示):
- 样本板
- 连结板
- 膜
- 吸收板,也称为吸液板
测试条通常由不同的组件(板和膜)组装而成。测试条外有一层塑料保护壳 (参考文献3)。
测试板和膜是多孔结构的。孔壁应该会被样本液润湿。样本可以在被施加到测试条上之前制备,也可以在样本板中制备。通过将血液或唾液与缓冲液混合来获取样本。缓冲液可能含有参考抗体和其他化学物质,例如能够确保样本润湿不同组分孔壁的溶剂。
样本板用于接收样本液滴,并充当流动的分配器和过滤器。非常大的蛋白质和血液细胞会被截获在样本板的多孔结构中。此外,多孔结构确保了样本液体能够沿板的宽度均匀分布。一旦样本充满了样本板,它就会继续向连结板的方向流动,流动是由液体与孔壁的相互作用引起的毛细管力驱动的。
在连结板中,过滤后的样本会溶解试剂,即所谓的“连结标签”,这些试剂在制造过程中已经被施加到连结板上。标签通常附着在例如金纳米粒子表面的抗原上。抗原可能是一种在免疫系统中能引发抗体的蛋白质。这些标签可以附着在样本中的抗体上,形成抗体和连结标签的络合物。络合物会溶解在样本液中,它们可以由附着在患者抗体上的标签和附着在制备过程中混合在样本中的参考抗体上的标签组成。一旦样本液填满了连结板中的孔,就会继续到抵达膜的位置,再次由毛细管力驱动前进。
样本液继续流过膜。膜通常由多孔硝酸纤维素制成,但也可以使用其他材料制备。不同的蛋白质和化学物质也可能与多孔膜的孔壁产生相互作用。一些物质可能在孔壁上被吸附和解吸。这种相互作用倾向于沿着流道分离不同的物质,这取决于物质分子的大小以及它们与孔表面相互作用的亲和力。这种作用被称为“免疫层析”。
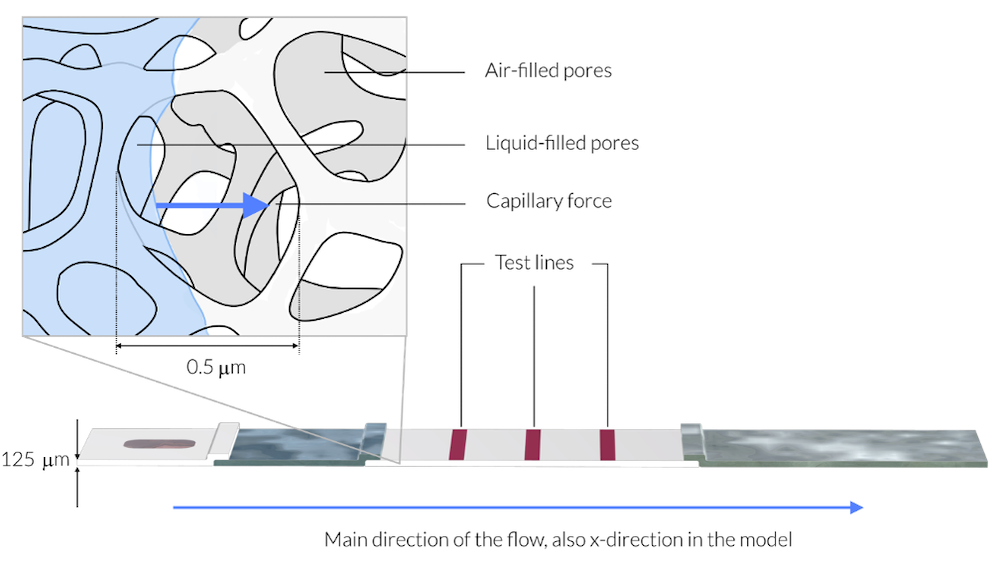
在这幅图中,样本液体刚刚到达膜的位置。放大显示为一个边长约 1µm 的矩形。平均孔径约为 0.5µm。作为比较,膜的厚度为 125µm (参考文献3)。液体样本用浅蓝色表示。膜由固态网格组成,像骨架一样,孔占膜体积的 70%。样本液体润湿骨架结构的壁,即孔壁,并在毛细管作用力的驱动下沿蓝色箭头指示的方向进入充满空气的孔中。请注意,为了清晰起见,该图中测试条的厚度被放大了 5 倍。
一旦样本与测试线接触,其中的一种络合物中就可以附着到测试线区域中存在的特定表面物质上。这种表面物质可以是固定在测试线表面的抗体。每条测试线可以连接一种特定的络合物。注意,表面物质在测试线区域是静止的;它既不溶解也不会被样品运输。一旦络合物附着到测试线上,测试线的区域就会改变颜色。颜色显示出特定抗体的特定络合物已经附着到特定测试线上了。
膜中的最后一条测试线是控制线。由于参考抗体总是被混合到样本中,因此控制线应该总是能检测到参考抗体与结合化学物质的复合物的存在。如果控制线没有检测到这种复合物,那么这意味着样本没有以正确的方式通过测试条,所以该次测试应该被视为无效。
当样本充满膜后,它会继续流向吸收板,吸收板起到吸液芯的作用。吸收板吸收样本,这种吸力驱使样本通过测试条,直到吸收板内完全充满样本。
模型预览
在本系列的下一篇博文中,我们将展示LFA设备的两种模型。这些模型揭示了一些由从事这些测试设计的科学家通过实验观察到的特征。其中一个特征是:流动如何取决于液体样本孔隙体积的饱和度?敬请关注后续博文!
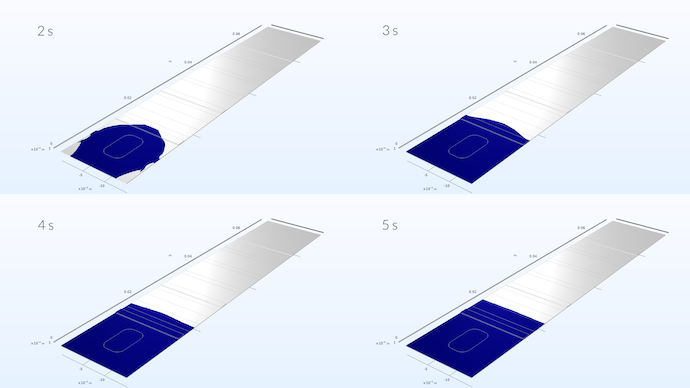
测试条中液体样本的扩散。模拟显示,一旦样本达到连接板的三分之一,样本就会形成均匀的速度分布。
参考文献
- T. Kilic, R. Weissleder, and H. Lee, “Molecular and Immunological Diagnostic Tests of COVID-19: Current Status and Challenges”,iScience, vol. 23, no. 101406, 2020, (https://www.cell.com/iscience/pdf/S2589-0042(20)30596-4.pdf).
- B.G. Andryukov, “Six decades of lateral flow immunoassay: from determining metabolic markers to diagnosing COVID-19”,AIMS Microbiology, vol. 6, no. 3, pp. 280–304, 2020, (https://pubmed.ncbi.nlm.nih.gov/33134745/).
- “Rapid Lateral Flow Test Strips, Considerations for Product Development”,Merck Millipore, 2013 EMD Millipore Corporation, Billerica, MA, USA.



评论 (0)