
等离子体化学对等离子体建模非常重要。例如,通过反应和碰撞才能明确等离子体中不同物质之间的相互作用。有了这些信息,就可以计算物质传输方程中出现的源项和传递系数。这篇博客,我们将介绍等离子体化学的组成部分,在哪里以及如何获取等离子体建模的相关数据。我们还将讨论制备等离子体化学的方法。
目录
等离子体化学组件
在低电离度的低温等离子体中,主要的物质是中性物质。这意味着电子和离子在是中性气体背景中传输(它们主要与之碰撞)的。对于我们感兴趣的等离子体建模,电子的能量要比等离子体中的所有其他物质高得多,电子平均能量约为几个电子伏特,背景气体的温度范围在室温到 1000 K 左右。
在许多工业反应堆中,等离子体通过施加一个能够将电子加速到可能发生电离的能量的电场来维持。在这种情况下,电子可以被认为是维持放电的主要载体,因为它们从电场中获得能量,并在与背景气体的碰撞中失去能量,反应产物可以是中性激发态、电子和离子。激发态和离子等重物质也会发生碰撞,导致电荷转移、电离和离子-离子复合。在等离子体反应器中,物质通过扩散和迁移进行运输,最终到达表面。需要描述与表面的相互作用。例如,假设电子在到达金属表面时被吸收并且离子被中和到基态是正常的。
总之,等离子体化学的主要元素是物质和性质,包括传输系数、电子撞击反应、重物质反应和表面反应。下面我们来更详细地讨论这些内容。
电子碰撞反应
电子碰撞反应可分为弹性、激发、电离或附着。我们可以使用 COMSOL Multiphysics®仿真软件中的电子碰撞反应功能定义这些类型的反应。下图是氧气电离反应的设置。
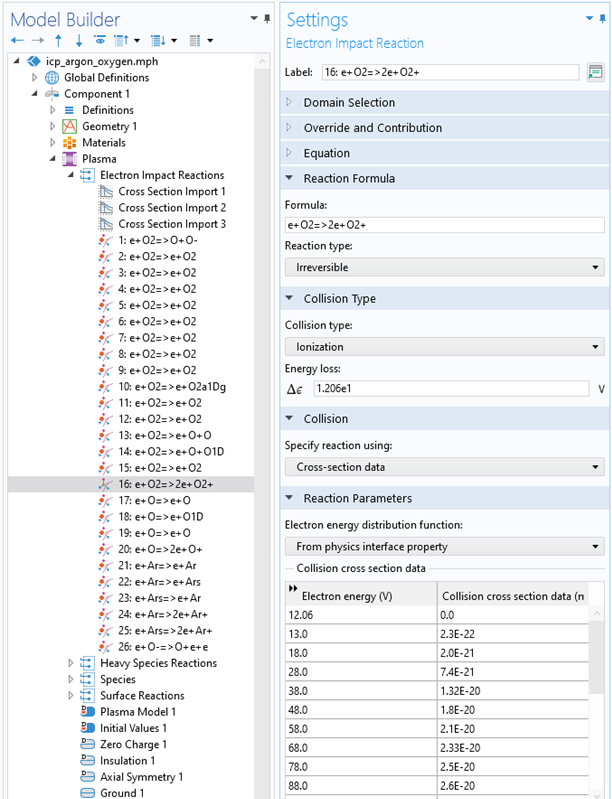
图1 模型开发器显示了用户定义的氩气和氧气混合物的等离子体化学的电子碰撞反应功能。设置窗口显示了电离分子氧的电子碰撞反应功能。反应由电子碰撞截面指定。
在弹性碰撞中,不会产生新的物质,但是电子和中性气体之间存在能量转移。在等离子体接口中设置弹性电子碰撞反应时,电子平均能量方程考虑了电子能量损失。此外,还创建了背景中性气体的热源项,并可以与流体传热接口耦合。在激发反应中,电子可以产生具有更高内能的新物质。逆反应也是可能的,在这种情况下,物质去激发,电子获得其能量。电离反应是激发的特例,因为会产生电子离子对。在电子附着反应中,电子被物质捕获,并产生负离子。这种类型的反应往往会非常有效地破坏低能量的电子。
在等离子体接口和等离子体,时间周期接口中,在定义电子碰撞反应时,将自动添加对所涉及物质连续性方程的源项的贡献,并将电子损失或获得的能量添加到电子平均能量方程的源项中。
传输方程中的源项是使用表示碰撞效应的速率系数计算的。获得电子速率系数的最佳策略是提供电子撞击截面,并在电子能量分布函数(EEDF)上进行适当的积分。原因是电子能量分布函数不是预先已知的,并且在低温等离子体中,电子能量分布函数经常偏离麦克斯韦电子能量分布函数。通过提供电子碰撞截面,可以保持改变电子能量分布函数的灵活性。
在 COMSOL®中,设置解析电子能量分布函数、导入电子能量分布函数或使用玻尔兹曼方程,两项近似接口计算电子能量分布函数都非常简单。
我们建议使用LXCat 数据库来获取电子碰撞截面。参考文献1 中讨论了如何获取流动类型模型的源项以及如何计算电子能量分布函数。
重物质反应
在模拟等离子体时,了解重物质之间的反应也很重要。参考文献2 和 3 对这一主题做了介绍。在这里,我们只介绍几种反应类型,用于说明重物质之间可能存在的相互作用。COMSOL®中的反应功能可以轻松定义重物质反应。图2 显示了使用速率常数定义离子-离子复合反应的设置窗口。
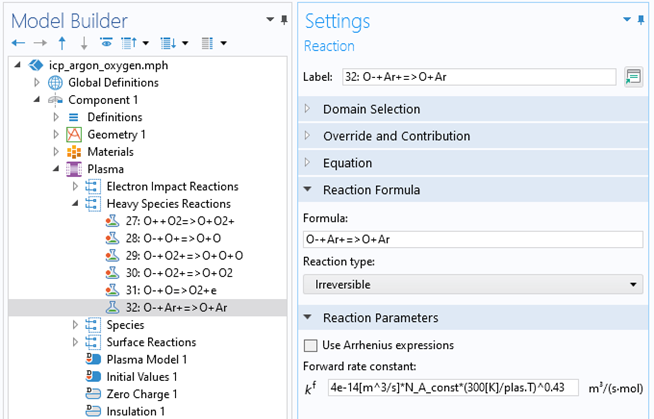
图2 模型开发器显示了用户定义的氩气和氧气混合物的等离子体化学的反应功能。设置窗口用于指定氧离子和氩离子之间的离子-离子复合的反应。
当其中一个物质的电子激发能大于另一个物质的电离势时,就会发生潘宁电离(A*+ A*=> e + A++ A)。在电荷转移反应 (A++ B => A + B+) 中,来自中性物质的电子转移到正离子或从负离子转移到中性粒子。在离子-离子复合(A–+ B+=> A + B) 中,负离子和正离子相互作用并产生中性物质。对于某些操作条件,这是描述负放电所必需的负离子损失机制。
涉及分子种类的等离子体化学更为复杂,因为电子碰撞和重物质缔合反应的解离创造了非常丰富的原子和分子物质系统。例如,在原料气体为 SF6,O2和 Ar 的放电过程中,像 F 和 SOx,SFx和 SOx等族新物质也会存在。
表面反应
在 COMSOL Multiphysics 中,使用表面反应功能指定重物质的表面反应,如图 3 所示。这个功能会自动为重物质设置与物质热速度成比例的通量边界条件。
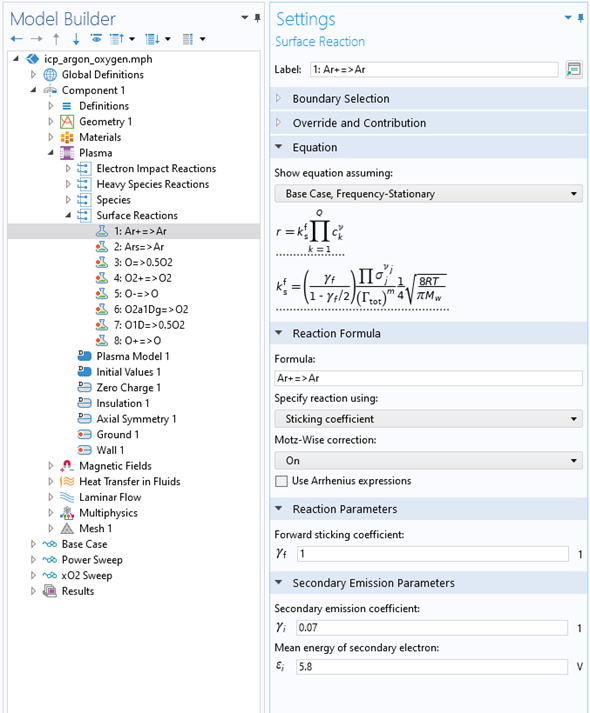
图3 模型开发器显示了用户自定义的氩气和氧气混合物的等离子体化学的表面反应功能。设置窗口显示了表面反应功能,用于指定表面氩离子的中和以及二次电子的发射。
下面,我们从等离子体的角度介绍一些重要的表面反应。讨论了表面物质的产生和损失,但我们没有具体介绍某种物质的表面反应或体反应发生了什么。(有关后者的更多信息,请尝试使用等离子体模块的表面化学反应教程模型)。
传输损失
在等离子体反应器中,通过平衡产生机制与体积和表面损失来实现稳态操作。通常,表面损失是主要机制。在实践中,这意味着电子碰撞反应会产生电子-离子对;电子在表面被吸收,而离子被中和到基态。如果没有为给定物质(包括激发态)引入损失机制,那么该物质可以无限生长。因此,无法实现稳态,导致数值模拟失败。图3 显示了如何使用表面反应功能 为离子 Ar+施加边界条件,并指定离子在表面被中和为基态 Ar。这是通过在公式字段中键入Ar+=>Ar来完成的。类似地,Ars=>Ar下面的反应表明激发态或氩Ars被解激发到基态。
电子二次发射
当离子或中性激发物质到达表面时,可以发射电子。这种电子产生机制对于直流(DC)放电的操作以及在电容耦合等离子体(CCP)反应堆中实现高功率状态(也称为γ 态)至关重要。通过在二次发射系数字段中指定一个不同于零的数字,可以很容易地在 COMSOL®中引入这种机制。在图3中,这个选项设置为 0.07,这意味着表面的离子通量乘以 0.07,并作为电子的通量源给出。
表面复合
在分子放电中,电子碰撞反应在将分子解离成其成分方面非常有效。在表面上,可能会发生重组。这种机制对于确定放电的解离程度很重要。对于氧气,通过在公式字段中键入O=>0.5O2并在正反应黏附系数字段中指定复合概率来设置表面复合。
传输系数
COMSOL®中使用的流动模型需要模型中所有物质的传输系数。主要的传输机制是电场中的扩散和迁移。这些传输机制由迁移率和扩散系数表征。对传输损失的良好估计需要准确的传输系数。对于电子,迁移率在电子如何从电场吸收能量方面起着重要作用。
电子传输系数
电子迁移率和扩散系数可以使用电子碰撞截面和EEDF 知识来计算。描述 EEDF 的常用方法是求解玻尔兹曼方程的近似形式。在 COMSOL Multiphysics 中,我们可以使用玻尔兹曼方程,两项近似接口来完成,该接口专用于求解两项近似中的玻尔兹曼方程。这样可以获得电子传输系数和源项。参考文献1 介绍了在两项近似中求解玻尔兹曼方程时使用的理论和近似。
重物质传递系数
对于所有重物质,等离子体接口中的默认设置是基于动力学理论计算扩散系数。用于计算扩散系数的方程使用了每种物质的摩尔质量、势特征长度、势能最小值和偶极矩。(你可以在参考文献4和等离子体模块用户指南文档的物质传递属性部分了解有关此方程的更多信息)。你可以手动引入此信息,也可以使用预设物质,如图4所示。对于离子,默认情况下,使用扩散系数和爱因斯坦关系计算物质迁移率。但是,也可以选择指定迁移率并使用爱因斯坦关系计算扩散系数。要了解如何将离子迁移率用作一般意义上的电场函数,请参阅参考文献5。
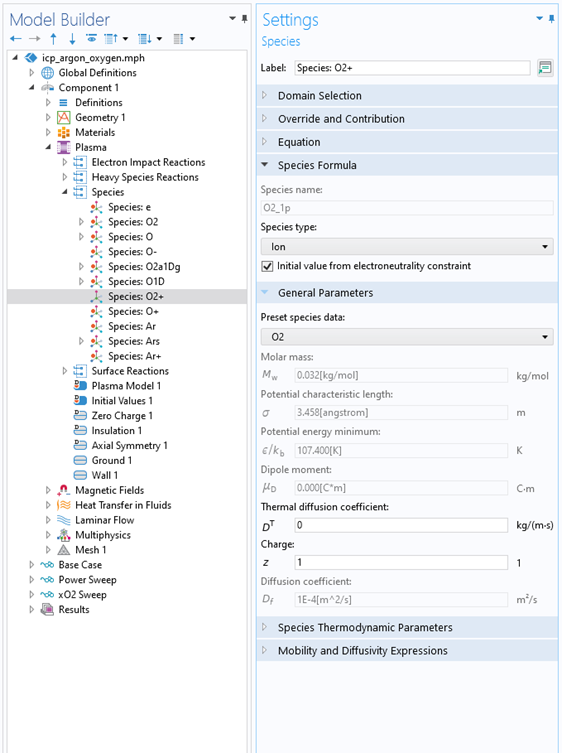
图4模型开发器显示了用户定义的氩气和氧气混合物的等离子体化学物质的功能。
数据来源
如果没有等离子体化学和相关数据,也可能很难获得。需要大量的文献研究,在许多情况下也需要大量的猜测工作。在这里,我们重点介绍可用于查找与等离子体化学相关的数据的参考文献。例如,参考文献6介绍了如何开发等离子体化学。作者还提供了等离子体化学数据的其他参考资料,并讨论了如何估算数据。参考文献2和参考文献3是关于等离子体物理和等离子体化学的教科书,并提供等离子体化学数据。参考文献5包含将离子迁移率用作电场函数的示例。为了获得电子碰撞反应,我们建议使用LXCat 数据库。
获得完整的等离子体化学的最简单方法是找到一篇已经完成的论文。参考文献7和参考文献8 中提供了这方面的一个例子,作者分别介绍并讨论了氩氧混合物和氯等离子体的等离子体化学成分。作者使用全局模型来研究化学物质,并使用实验结果进行验证。
开发等离子体化学的工作流程
等离子体化学通常用于对等离子体反应器进行建模。但是,最好将等离子体化学的制备与反应器模型的创建分开。设置反应器模型时,建议使用简单的等离子体化学(如下面示例1 部分中的化学成分)以避免与等离子体化学相关的问题。这样做将使你能够专注于仿真的其他方面,例如:
- 研究激励源如何与系统耦合
- 寻找优质网格
- 设置与其他流体流动和传热接口的耦合
- 寻找适当的边界条件
- 确定求解器策略
在准备等离子体化学时,第一步是获得一组电子碰撞反应,对于反应器的运行条件,使用玻尔兹曼方程,两项近似接口计算电子传输参数和源项。这个步骤应该会使你对截面集充满信心;为此,应严格分析计算出的 EEDF、源项和传输系数。在这个步骤中获得的传输参数、源项和 EEDF 稍后可以在等离子体接口或等离子体,时间周期接口中使用。干空气玻尔兹曼分析模型中对这个步骤做了很好的示例。
第二步是准备一个全局模型来测试和验证化学。在全局模型中,等离子体反应器中不同数量的空间信息可以视为是均匀的,也可以使用解析模型引入。如果没有空间导数,该模型由一组常微分方程(ODE)组成。因此,数值解变得相当简单,计算时间也减少了。全局模型应包括先前测试的截面以及等离子体化学的所有其他组成部分;氯放电全局模型示例介绍了如何为全局模型添加化学成分。
对于非常大的化学反应,最好以小步骤添加反应和物质,并验证模型是否仍能求解。在步骤中添加化学元素时,可能需要调整初始条件和操作条件以获得收敛性。在连贯的组中添加新元素也很重要。以下是一些例子:
- 如果加入解离反应,例如 e + O2=> e + O + O,添加体积和表面复合反应也很重要。
- 如果反应 e + Ar=> e + Ar*产生新的激发态 Ar*,则添加 Ar*的表面和体积损失,并研究逐步电离是否重要。
- 如果产生负离子,则添加体积反应以破坏负离子,因为传输造成的损失通常可以忽略不计。
在电子碰撞反应中,产物可以是激发态,但可能不需要明确求解激发态。减少空间相关模型中求解的激发态数量是一种常见的策略,可以先在全局模型中进行测试。在 COMSOL®中,如果在等离子体接口中添加类似 e + N2 => e + N2(A3)的反应,则物质 N2(A3)及其传输方程会自动相加。因此,如果不需要明确处理激发态,则可以简单地将反应式更改为e + N2 => e + N2。这样,电子仍然会失去能量并改变截面指定的动量,但不会产生激发态。或者,可以将几个激发态放在一起,并用通用态 N2 表示它们。为此,反应 e + N2 => e + N2(A3)和产生相似状态的反应更改为 e + N2 => e + N2。**
最后一步,应将使用全局模型测试和验证的等离子体化学添加到空间相关模型中。这一步很重要,因为即使已经测试了化学成分,空间相关模型也包含与物质迁移相关的现象,这些现象在测试中没有考虑,并且可能导致模型失败。例如,在负电放电中,负离子密度往往具有非常尖锐的过渡区域,难以求解。你可以通过氩/氧电感耦合等离子体反应器模型和氩/氧电容耦合等离子体反应器模型教程了解电负放电建模的重要因素和策略。
等离子体化学示例
在准备等离子体化学之前,确定要从模型中学习的内容非常重要。如果你正在使用可以接受大公差的模型,并且想要计算等离子体的均匀性、功率吸收、气体加热或电极上的电流,那么简化的化学反应(如以下示例中所示)是一个很好的起点。使用这种化学方法是有好处的,因为一般的想法是使等离子体化学尽可能简单。但是,如果你正在使用的模型需要更严格的公差,并且你希望了解特定的激发态,那就需要更精细的化学成分,例如参考文献7中介绍的化学成分。
示例1
图5显示了一个在等离子体接口中实现的氩等离子体的简单化学反应的示例。在准备反应器模型时,建议使用这样的化学成分。它可以在 COMSOL 案例库的许多模型中找到,例如直流辉光放电模型。这种化学有四种物质,包括电子、基态、有效激发态和离子。电子碰撞截面描述的电子碰撞反应有 5 种:与基态的弹性碰撞,对 Ars 的激发,Ars 的去激发,从基态电离和激发态的电离。使用反应特征包括潘宁电离和 Ars 态的淬灭。在表面,离子被中和,Ars 去激发至基态。
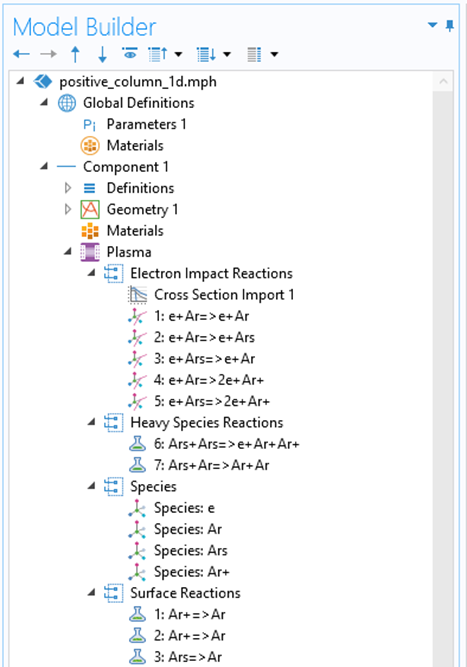
图5 氩气的等离子体化学。
COMSOL Multiphysics 用户界面特写图,显示了模型开发器与扩展的等离子体接口,显示了氩气的等离子体化学特性。
示例2
图6 显示了氩气和氧气混合物中等离子体的化学成分。该化学反应用于氩/氧电感耦合等离子体反应器模型和氩/氧电容耦合等离子体反应器教程模型,旨在为氩气-氧气混合物提供基础化学,可以添加更多反应。氩气反应与示例1相同。请注意,氧反应基于参考文献2和参考文献7,所有电子碰撞截面均来自 LXCat。
许多由电子碰撞反应产生的激发态不包括在产品中,以确保不会产生新物质。(在等离子体接口中,如果在反应中添加新物质,则会自动添加因变量和传递方程)。只添加了分子氧和原子氧的两种亚稳态,并且两个反应是解离的,导致产生原子氧。即使电子碰撞反应不会产生新的物质,电子损失的能量仍然在电子平均能量方程中得到考虑。
氧是一种电负性物质,这意味着电子可以附着并产生负离子(电子撞击反应1)。即使负离子包括表面反应,其通过传输损失也可以忽略不计,并且需要包括体积损失(重物质反应 28-32)。
解离度是分子放电的一个重要方面。当然,原子氧含量较高的放电的电负性较小,因为附着电子的分子氧较少。在这种化学反应中,仅包括表面缔合机制(表面反应3和7),它们对于维持实际解离度至关重要。
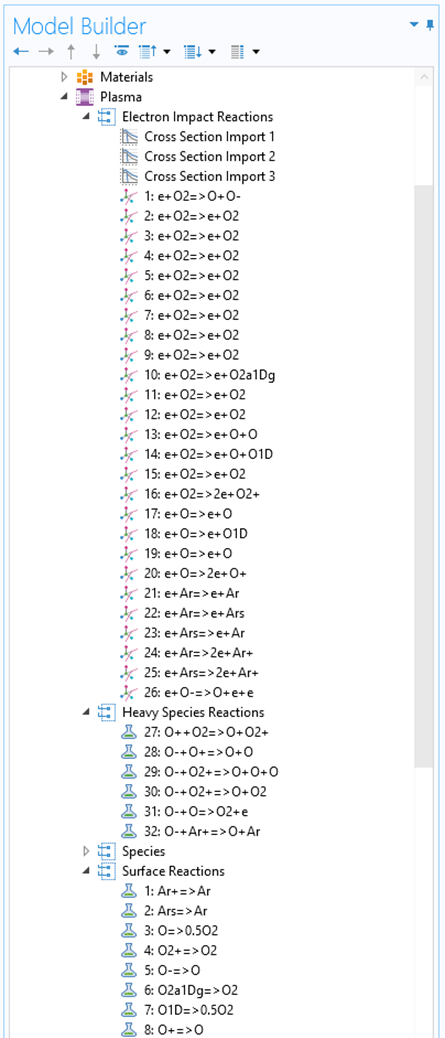
图6 氩气和氧气混合物的等离子体化学反应。
下一步
欢迎尝试使用本博客中链接的各种模型在 COMSOL Multiphysics 中设置等离子体。如果你对等离子体建模有任何疑问,请通过以下按钮联系 COMSOL。
参考文献
- G.J.M. Hagelaar and L. C. Pitchford, “Solving the Boltzmann equation to obtain electron transport coefficients and rate coefficients for fluid models,”Plasma Sources Science and Technology, vol. 14, pp. 722–733, 2005.
- M.A. Lieberman and A.J. Lichtenberg,Principles of Plasma Discharges and Materials Processing, John Wiley & Sons, 2005.
- A. Friedman,Plasma Chemistry, Cambridge University Press, 2008.
- R.J. Kee, M.E. Coltrin, and P. Glarborg,Chemically Reacting Flow Theory and Practice, Wiley, 2003.
- H.W. Ellis et al., “Transport properties of gaseous ions over a wide energy range,” Parts I–III,Atomic Data and Nuclear Data Tables, vol. 17, pp. 177–210, 1976; vol. 22, pp. 179–217, 1978; vol. 31, pp. 113–151, 1984.
- M.J. Kushner, “Strategies for Rapidly Developing Plasma Chemistry Models,”Bull. Am. Phys. Soc., 1999.
- J.T. Gudmundsson and E.G. Thorsteinsson, “Oxygen discharges diluted with argon: dissociation process,”Plasma Sources Science and Technology, vol. 16, pp. 399–412, 2007.
- E.G. Thorsteinsson and J.T. Gudmundsson, “A global (volume averaged) model of a chlorine discharge,”Plasma Sources Science and Technology, vol. 19, p. 15, 2010.



评论 (0)