你的化学老师曾经拿出橙子或者柠檬来解释电池的概念吗?也许你还记得,当他把几根金属钉插进了柑橘类水果后,居然成功地发出了电!整个班的同学都目不转睛地盯住这个迷你发电机。如果我们现在使用仿真工具来演示橙子电池的工作原理,然后将它用作电化学建模的入门教程,效果会怎样呢?
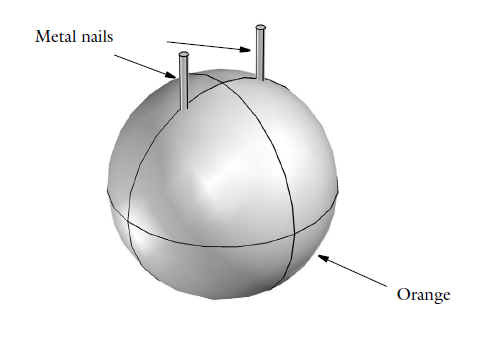
橙子电池的几何结构。
橙子电池的工作原理
橙子电池能发电,这显然不是魔法,而是神奇的电化学。橙子属于柑橘类水果,含有柠檬酸,柠檬酸和其他离子共同充当了电解质。两根金属钉必须由不同的金属制成,分别用于释放和获得电子,保证电化学反应的进行。完整的电路需要两根钉子通过一个金属导体(例如可以在学校实验室中轻易找到的小电灯泡)进行电连接。在这个过程中,钉子充当了电极,电池(此处为橙子)中存在着有利于促进电子转移的电偶电位。因为我们正在利用化学反应将化学能转化为电能,所以也可以将橙子电池称作伏打电池,就像其他将能量储存在化学物质中的电池一样。
Galvani 和青蛙发明了世界上第一个电池
一个有趣的事实:意大利物理学家路易吉·加尔瓦尼(Luigi Galvani)发现了“动物电”——当时他将两种不同的金属串接在一条青蛙腿上,青蛙开始剧烈痉挛。实际上这是由离子运动引起的。意大利物理学家亚历山德罗·沃尔塔(Alessandro Volta)对此很感兴趣,经过反复实验得出结论:青蛙的腿既担当了导体,又是电检测器。在这项研究的基础上,他最终提出了所谓的 Volta 定律的电化学系列,后来到 19 世纪,世界上第一个电池诞生了。
电化学建模:以橙子电池为例
如果您是电化学应用建模的新手,可能需要从橙子电池模型教程开始。按照 PDF 中的分步指导,我们可以模拟橙子电池中的电流和溶解的金属离子浓度。
模型中的两根钉子分别由锌和铜制成。锌钉在电极反应中失去电子,反应式如下:
Zn(s) → Zn2+2e–E0= –0.82V
随后,锌离子流入电池电解质。与此同时,铜钉起着电催化剂的作用,促进了如下析氢反应,氢离子来自柠檬酸:
2H++ 2e–→ H2(g) E0= 0V
二次电流分布接口可以用于创建橙子和电极内电流的模型。二次电流分布假设电解质只通过离子迁移来传递电荷,电极反应则是电势和局部反应物质浓度的函数。因此,欧姆定律与电荷守恒定律一起被用来求解金属钉和橙子电解质中的电流,电流也与描述电化学反应的 Butler-Volmer 表达式相互耦合。在本示例中,我们将一根金属钉上的电位设置为该单元电池的电位0.5V,另一根金属钉接地,据此来计算电流分布。
只要我们创建并求解了该模型,就能计算橙子电池的性能。
 |
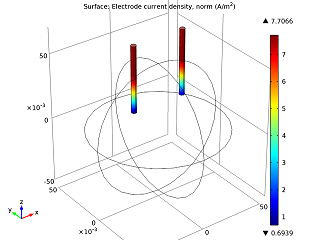 |
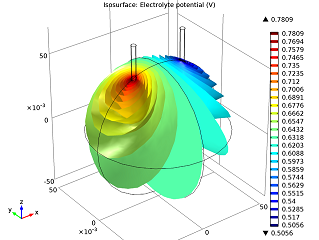
| 电解质的电势场。 | 钉子的电流。 |
从上方左图中可以看出,随着电流从锌电极(左边的钉子)流向铜电极(右边的钉子),电势逐渐下降。电池电压损耗主要来源于电解质中的欧姆损耗。如果要提升电池的性能,可以把橙子换成电导率更高(酸含量更多)的水果,比如柠檬,或者把钉子靠得更近。在上方模型中,电流沿 z 轴逐渐增大。这是因为在电极的末端,接触的橙子体积更多,反应物质更充足,因此更容易得到和失去电子。
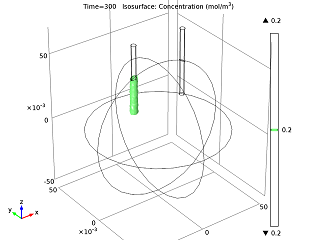
我们还可以研究电池运行一段时间后的离子浓度水平,并绘制电池电流随时间的变化情况。当锌离子逐渐积聚后,会阻碍阳极的反应能力,因此电池电流逐渐降低,直到电流密度达到恒定水平。
 |
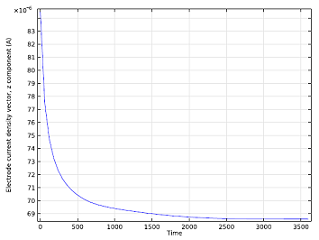 |
| 当电池运行 5 分钟后,锌离子浓度为 0.2 mol / m3时的等值面图。 | 电池电流与时间的关系。 |



评论 (0)